en
names in breadcrumbs


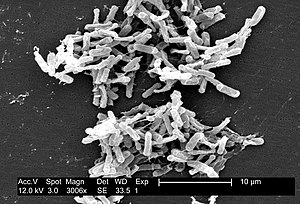
C. absonum
C. aceticum
C. acetireducens
C. acetobutylicum
C. acidisoli
C. aciditolerans
C. acidurici
C. aerotolerans
C. aestuarii
C. akagii
C. aldenense
C. aldrichii
C. algidicarnis
C. algidixylanolyticum
C. algifaecis
C. algoriphilum
C. alkalicellulosi
C. aminophilum
C. aminovalericum
C. amygdalinum
C. amylolyticum
C. arbusti
C. arcticum
C. argentinense
C. asparagiforme
C. aurantibutyricum
C. baratii
C. barkeri
C. bartlettii
C. beijerinckii
C. bifermentans
C. bolteae
C. bornimense
C. botulinum
C. bowmanii
C. bryantii
C. butyricum
C. cadaveris
C. caenicola
C. caminithermale
C. carboxidivorans
C. carnis
C. cavendishii
C. celatum
C. celerecrescens
C. cellobioparum
C. cellulofermentans
C. cellulolyticum
C. cellulosi
C. cellulovorans
C. chartatabidum
C. chauvoei
C. chromiireducens
C. citroniae
C. clariflavum
C. clostridioforme
C. coccoides
C. cochlearium
C. cocleatum
C. colicanis
C. colinum
C. collagenovorans
C. cylindrosporum
C. difficile
C. diolis
C. disporicum
C. drakei
C. durum
C. estertheticum
C. fallax
C. felsineum
C. fervidum
C. fimetarium
C. formicaceticum
C. frigidicarnis
C. frigoris
C. ganghwense
C. gasigenes
C. ghonii
C. glycolicum
C. glycyrrhizinilyticum
C. grantii
C. haemolyticum
C. halophilum
C. hastiforme
C. hathewayi
C. herbivorans
C. hiranonis
C. histolyticum
C. homopropionicum
C. huakuii
C. hungatei
C. hydrogeniformans
C. hydroxybenzoicum
C. hylemonae
C. jejuense
C. indolis
C. innocuum
C. intestinale
C. irregulare
C. isatidis
C. josui
C. kluyveri
C. lactatifermentans
C. lacusfryxellense
C. laramiense
C. lavalense
C. lentocellum
C. lentoputrescens
C. leptum
C. limosum
C. litorale
C. lituseburense
C. ljungdahlii
C. lortetii
C. lundense
C. magnum
C. malenominatum
C. mangenotii
C. mayombei
C. methoxybenzovorans
C. methylpentosum
C. neopropionicum
C. nexile
C. nitrophenolicum
C. novyi
C. oceanicum
C. orbiscindens
C. oroticum
C. oxalicum
C. papyrosolvens
C. paradoxum
C. paraperfringens(Alias: C. welchii)
C. paraputrificum
C. pascui
C. pasteurianum
C. peptidivorans
C. perenne
C. perfringens
C. pfennigii
C. phytofermentans
C. piliforme
C. polysaccharolyticum
C. populeti
C. propionicum
C. proteoclasticum
C. proteolyticum
C. psychrophilum
C. puniceum
C. purinilyticum
C. putrefaciens
C. putrificum
C. quercicolum
C. quinii
C. ramosum
C. rectum
C. roseum
C. saccharobutylicum
C. saccharogumia
C. saccharolyticum
C. saccharoperbutylacetonicum
C. sardiniense
C. sartagoforme
C. scatologenes
C. schirmacherense
C. scindens
C. septicum
C. sordellii
C. sphenoides
C. spiroforme
C. sporogenes
C. sporosphaeroides
C. stercorarium
C. sticklandii
C. straminisolvens
C. subterminale
C. sufflavum
C. sulfidigenes
C. symbiosum
C. tagluense
C. tepidiprofundi
C. termitidis
C. tertium
C. tetani
C. tetanomorphum
C. thermaceticum
C. thermautotrophicum
C. thermoalcaliphilum
C. thermobutyricum
C. thermocellum
C. thermocopriae
C. thermohydrosulfuricum
C. thermolacticum
C. thermopalmarium
C. thermopapyrolyticum
C. thermosaccharolyticum
C. thermosuccinogenes
C. thermosulfurigenes
C. thiosulfatireducens
C. tyrobutyricum
C. uliginosum
C. ultunense
C. villosum
C. vincentii
C. viride
C. xylanolyticum
C. xylanovorans
クロストリジウム属(Clostridium)は、真正細菌の一属である。偏性嫌気性で芽胞を形成するグラム陽性の桿菌である[1][2]。この属名は、ギリシャ語のkloth(捻じれ)から派生したklostridion(小さい捻じれたもの)から来ており、ラテン語化するとClostridium となる[3]。
クロストリジウム属の菌は、土壌内部や生物の腸内などの酸素濃度が低い環境に生息する偏性嫌気性菌であり、酸素存在下では増殖できない。一般に偏性嫌気性菌は、スーパーオキシドディスムターゼやカタラーゼなどの活性酸素を無毒化する酵素を持たないため、酸素がある通常の環境下では不活化するが、クロストリジウム属細菌は酸素存在下で、耐久性の高い芽胞を作って休眠することで、死滅を免れることができる。この性質から、他の偏性嫌気性菌が生き残れない状態でも生き残るため、偏性嫌気性菌の中では比較的古くからその存在が発見され、研究が進められてきた。
ハイム・ワイツマン(後にイスラエル初代大統領)による1919年の特許[4]によりデンプンから発酵によって工業的な規模でのアセトン・ブタノール生産が可能になったが、この発酵に用いられたのもクロストリジウム属細菌であり、第一次世界大戦中は燃料や火薬の原材料として破砕したトウモロコシからアセトンを生産していた。この発酵生産法は化学合成法が発達する1950年代まで、アセトンやブタノールの主な生産法であった。
次のクロストリジウム属5種はヒトに対する病原性を有する。
このほか、C. novyiやC. septicumなどのガス壊疽菌群は傷口に感染して、重篤なガス壊疽を起こす。ガス壊疽が発生した際に、外科的な切除、抗菌薬の投与に加えて、クロストリジウム属が偏性嫌気性であることを利用して高気圧酸素治療が試みられることもある。
クロストリジウム属菌はガン細胞を選択的に攻撃することが知られており、また、いくつかの菌株は充実性腫瘍へ入り込んで増殖することができる。このため、非病原性のクロストリジウム属菌は腫瘍へと治療用タンパク質の運搬に利用できる可能性があり、実用化に向けた研究が進められている[21]。
病原性クロストリジウム属菌は、近年、医療分野においてその偏性嫌気性菌としての能力を利用したがん治療への応用が期待されている[22]。また、(Shaw 2010)によって、自閉症をもつ小児の尿より本属が作り出す物質3-(3-ヒドロキシフェニル)-3-ヒドロキシプロパン酸(略称:HPHPA) が高濃度で検出される報告がなされ、カビ毒の向神経作用が注目された。
C. beijerinckiiやC. butyricum等の混合体は廃酵母から水素[ 英: biohydrogen ]を産生する[23]
クロストリジウム属(Clostridium)は、真正細菌の一属である。偏性嫌気性で芽胞を形成するグラム陽性の桿菌である。この属名は、ギリシャ語のkloth(捻じれ)から派生したklostridion(小さい捻じれたもの)から来ており、ラテン語化するとClostridium となる。
クロストリジウム属の菌は、土壌内部や生物の腸内などの酸素濃度が低い環境に生息する偏性嫌気性菌であり、酸素存在下では増殖できない。一般に偏性嫌気性菌は、スーパーオキシドディスムターゼやカタラーゼなどの活性酸素を無毒化する酵素を持たないため、酸素がある通常の環境下では不活化するが、クロストリジウム属細菌は酸素存在下で、耐久性の高い芽胞を作って休眠することで、死滅を免れることができる。この性質から、他の偏性嫌気性菌が生き残れない状態でも生き残るため、偏性嫌気性菌の中では比較的古くからその存在が発見され、研究が進められてきた。
ハイム・ワイツマン(後にイスラエル初代大統領)による1919年の特許によりデンプンから発酵によって工業的な規模でのアセトン・ブタノール生産が可能になったが、この発酵に用いられたのもクロストリジウム属細菌であり、第一次世界大戦中は燃料や火薬の原材料として破砕したトウモロコシからアセトンを生産していた。この発酵生産法は化学合成法が発達する1950年代まで、アセトンやブタノールの主な生産法であった。